Filtración glomerular, flujo sanguíneo renal y
su control
Filtración glomerular, flujo sanguíneo renal y
su control
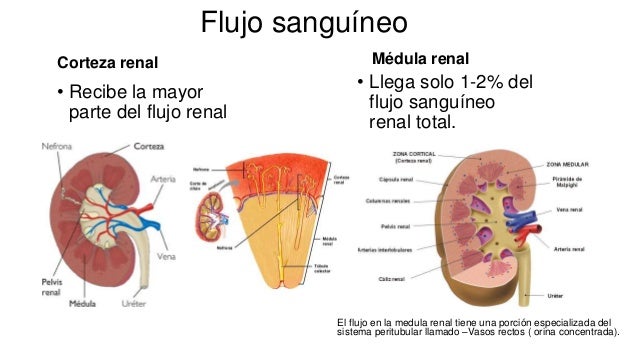
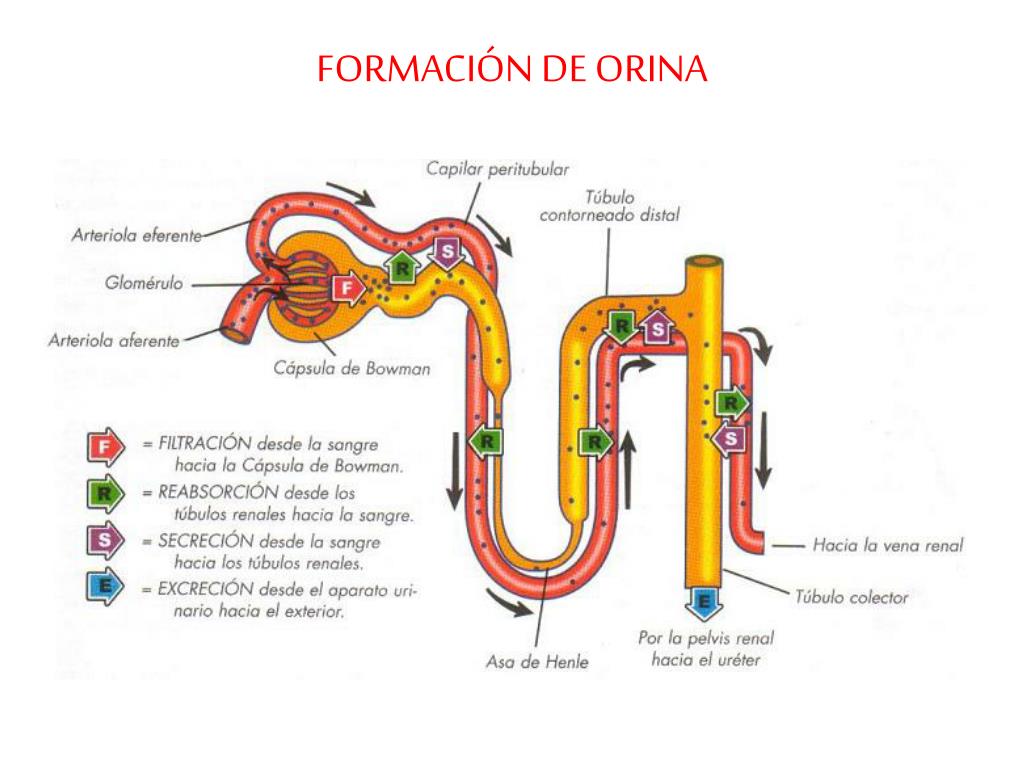
Filtración glomerular: el primer paso para la formación de orina
El primer paso en la formación de orina es la filtración de grandes cantidades de líquidos a través de los capilares glomerulares en la cápsula de Bowman, casi 180 l al día.
La mayor parte de este filtrado se reabsorbe, lo que deja únicamente 1 l aproximadamente de líquido para su excreción al día, si bien la tasa de excreción renal de líquidos puede ser muy variable dependiendo de la ingestión de líquidos.
La alta tasa de filtración glomerular depende de la alta tasa de flujo sanguíneo renal, así como de las propiedades especiales de las membranas de los capilares glomerulares.
Las concentraciones de otros constituyentes del filtrado glomerular, como la mayoría de las sales y moléculas orgánicas, son similares a las concentraciones en el plasma.
Las excepciones a esta generalización son algunas sustancias con un peso molecular bajo, como el calcio y los ácidos grasos, que no se filtran libremente porque están unidas parcialmente a las proteínas plasmáticas.

La FG está determinada por:
- El equilibrio entre las fuerzas hidrostáticas y coloidosmóticas que actúa a través de la membrana capilar
- El coeficiente de filtración capilar (Kf), el producto de la permeabilidad por el área superficial de filtro de los capilares. Los capilares glomerulares tienen una filtración mucho mayor que la mayoría de los otros capilares por una presión hidrostática glomerular alta y un gran Kf. En el adulto medio, la FG es de unos 125 ml/min, o 180 l/día.

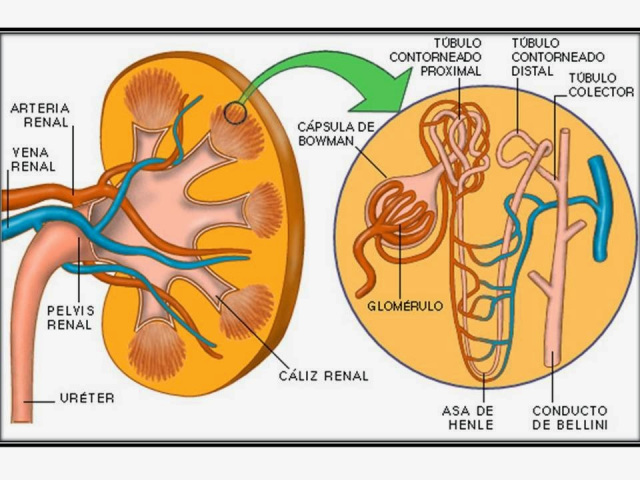
Membrana capilar glomerular
La membrana capilar glomerular es similar a la de otros capilares, excepto en que tiene tres capas principales (en lugar de las dos habituales):
- El endotelio del capilar
- Una membrana basal
- Una capa de células epiteliales (podocitos) rodeando a la superficie externa de la membrana basal capilar
El endotelio capilar está perforado por cientos de pequeños agujeros, llamados
fenestraciones, similares a los capilares fenestrados que se encuentran en el hígado, aunque menores que las fenestraciones del hígado.
Aunque la fenestración es relativamente grande, las proteínas
celulares endoteliales están dotadas de muchas cargas negativas fijas que dificultan el paso de las proteínas plasmáticas.
Rodeando al endotelio está la membrana basal, que consta de una red de colágeno y fibrillas deproteoglucanos que tienen grandes espacios a través de los cuales pueden filtrarse grandes cantidades de agua y de solutos.
La membrana basal evita con eficacia la filtración de proteínas plasmáticas, en
parte debido a las cargas eléctricas negativas fuertes de los proteoglucanos.
Los podocitos están separados por espacios llamados poros en hendidura a través de los cuales se mueve el filtrado glomerular.
Las células epiteliales, que tienen también cargas negativas, restringen de
forma adicional la filtración de las proteínas plasmáticas.

La membrana capilar glomerular es más gruesa que la de la mayoría de los otros capilares, pero es también mucho más porosa y por tanto filtra líquido con mayor intensidad. A pesar de la elevada filtración, la barrera de filtración glomerular filtra de modo selectivo las moléculas basándose en su tamaño y en su carga eléctrica.
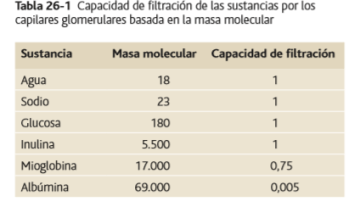
Una capacidad de filtración de 1 significa que la sustancia se filtra tan libremente como el agua; una capacidad de filtración de 0,75 significa que la sustancia se filtra con una rapidez de solo un 75% la del agua.
Determinantes de la FG

La FG está determinada por: 1) la suma de las fuerzas hidrostática y coloidosmótica a través de la membrana glomerular, que da lugar a la presión de filtración neta, y 2) el coeficiente glomerular Kf.
En una fórmula matemática, la FG es igual al producto del Kf y de la presión de filtración neta
La presión de filtración neta representa la suma de las fuerzas hidrostática y coloidosmótica que favorecen o se oponen a la filtración a través de los capilares glomerulares.
Estas fuerzas son:
- La presión hidrostática dentro de los capilares glomerulares (presión hidrostática glomerular, PG), que favorece la filtración
- La presión hidrostática en la cápsula de Bowman (PB) fuera de los capilares, que se opone a la filtración
- La presión coloidosmótica de las proteínas plasmáticas en el capilar glomerular (πG), que se opone a la filtración
- La presión coloidosmótica de las proteínas en la cápsula de Bowman (πB), que favorece la filtración.

El aumento del coeficiente de filtración capilar glomerular
incrementa la FG
El Kf es una medida del producto de la conductividad hidráulica y el área superficial de los capilares glomerulares.
Dado que la FG total en los dos riñones es de unos 125 ml/min y la presión de filtración neta 10 mmHg, el Kf normal se calcula en unos 12,5 ml/min/mmHg de presión de filtración.
Cuando el Kf se expresa por 100 g de peso renal, tiene un promedio de alrededor de 4,2 ml/min/mmHg, un valor unas 400 veces mayor que el Kf de la mayoría de los otros sistemas capilares del cuerpo; el Kf medio de la mayoría de los otros tejidos del cuerpo es solo de unos 0,01 ml/min/mmHg por 100 g.
Este Kf alto de los capilares glomerulares contribuye a su filtración rápida de líquido.
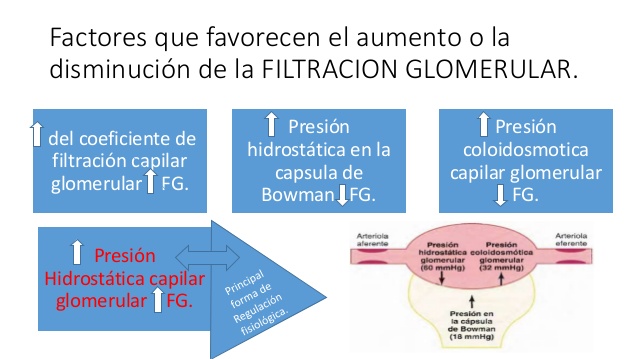
El aumento de la presión hidrostática en la cápsula de
Bowman reduce la FG
El aumento de la presión hidrostática en la cápsula de Bowman reduce la FG,
mientras que reducir la presión aumenta la FG. Pero los cambios en la presión de la cápsula de Bowman no son normalmente un mecanismo importante de regulación de la FG.
En ciertos estados patológicos asociados a la obstrucción de la vía urinaria, la presión en la cápsula de Bowman puede aumentar mucho y provocar una reducción grave de la FG.
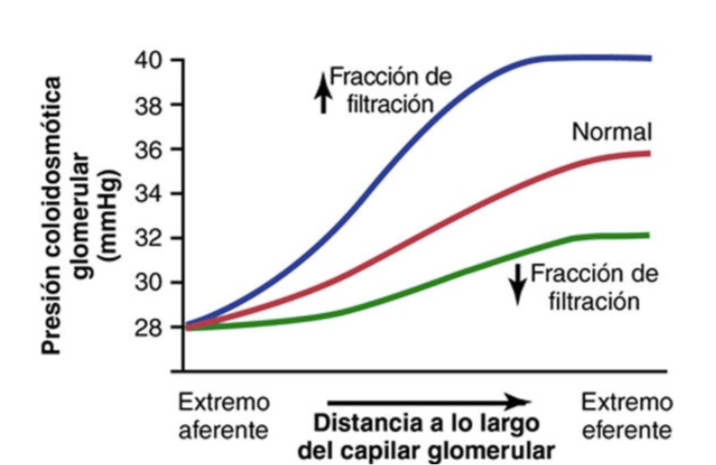
El aumento de la presión coloidosmótica capilar glomerular
reduce la FG
A medida que la sangre pasa desde la arteriola aferente a través de los capilares glomerulares hasta las arteriolas eferentes, la concentración plasmática de las proteínas aumenta alrededor de un 20%.
La razón de este aumento es que alrededor de una quinta parte del líquido en los capilares se filtra a la cápsula de Bowman, lo que concentra las proteínas plasmáticas glomerulares que no se filtran.
Suponiendo que la presión coloidosmótica normal del plasma que entra en los capilares glomerulares es de 28 mmHg,
El aumento de la presión hidrostática capilar glomerular
incrementa la FG
Se ha calculado que la presión hidrostática capilar glomerular es de unos 60 mmHg en condiciones normales.
Los cambios en la presión hidrostática glomerular son la principal forma de regular fisiológicamente la FG.
Los aumentos en la presión hidrostática glomerular incrementan la FG, mientras que las reducciones en la presión hidrostática glomerular la reducen.
La presión hidrostática glomerular está determinada por tres variables, todas ellas bajo control fisiológico:
- Presión arterial
- Resistencia arteriolar aferente
- Resistencia arteriolar eferente.
El aumento de la presión arterial tiende a elevar la presión hidrostática glomerular y, por tanto, a aumentar la FG.
La constricción de las arteriolas eferentes aumenta la resistencia al flujo de salida de los capilares
glomerulares. Este mecanismo incrementa la presión hidrostática glomerular, y mientras que el
aumento de la resistencia eferente no reduzca demasiado el flujo sanguíneo renal, la FG se eleva
ligeramente (
Flujo sanguíneo renal

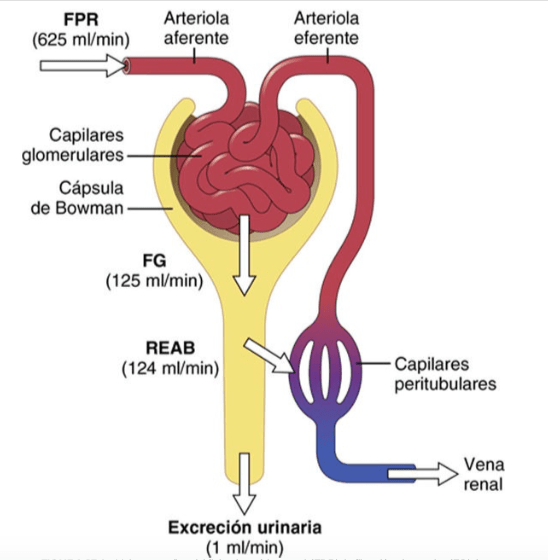
En un hombre de 70 kg, el flujo sanguíneo combinado a través de los dos riñones es de unos 1.100 ml/min, o un 22% del gasto cardíaco. Considerando el hecho de que los dos riñones constituyen solo alrededor del 0,4% del peso total del cuerpo, podemos percibir fácilmente que reciben un flujo extremadamente grande de sangre comparados con otros órganos.
Como en otros tejidos, el flujo sanguíneo aporta a los riñones nutrientes y se lleva los productos de desecho.
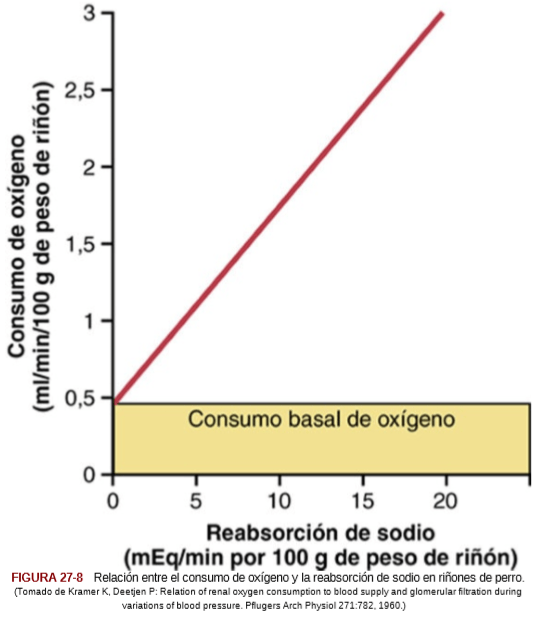
Flujo sanguíneo renal y consumo de oxígeno
Con respecto al gramo de peso, los riñones consumen normalmente el doble de oxígeno que el encéfalo, pero tienen casi siete veces más flujo sanguíneo.
Luego el oxígeno transportado a los riñones supera con mucho sus necesidades metabólicas, y la extracción arteriovenosa de oxígeno es relativamente baja comparada con la de la mayor parte de los restantes tejidos.
Una gran fracción del oxígeno consumido por los riñones se relaciona con la elevada reabsorción del sodio en los túbulos renales.
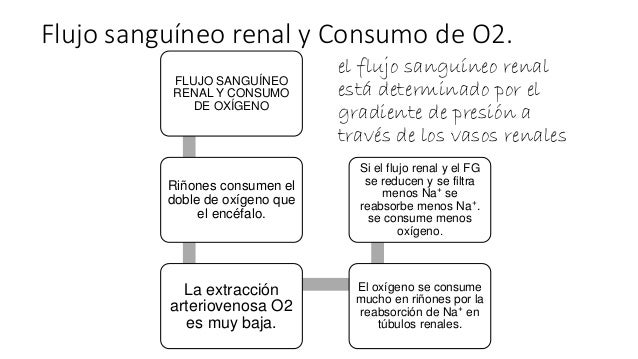
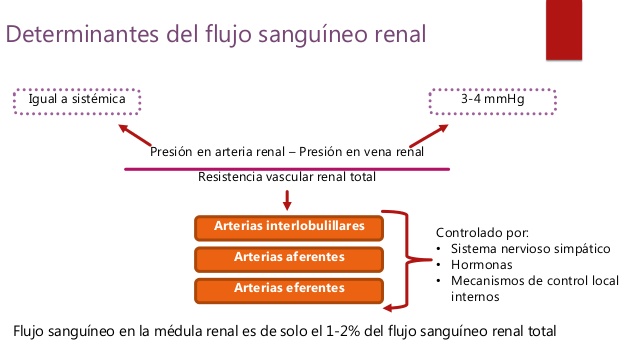
Determinantes del flujo sanguíneo renal
El flujo sanguíneo renal está determinado por el gradiente de presión a través de los vasos renales (la diferencia entre las presiones hidrostáticas en la arteria renal y en la vena renal), dividido entre la resistencia vascular total renal
La presión en la arteria renal es aproximadamente igual a la presión arterial sistémica, y la presión en la vena renal es de media de 3-4 mmHg en la mayoría de las condiciones.
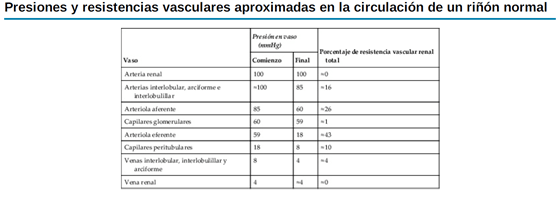
La mayor parte de la resistencia vascular renal reside en tres segmentos principales: las arterias
interlobulillares, las arterias aferentes y las arteriolas eferentes. La resistencia de estos vasos está
controlada por el sistema nervioso simpático, varias hormonas y mecanismos de control locales
internos, como se comentará más adelante. Un aumento de la resistencia en cualquiera de los
segmentos vasculares de los riñones tiende a reducir el flujo sanguíneo renal, mientras que una
reducción en la resistencia vascular aumenta el flujo sanguíneo renal si las presiones en la vena y
arteria renales permanecen constantes.
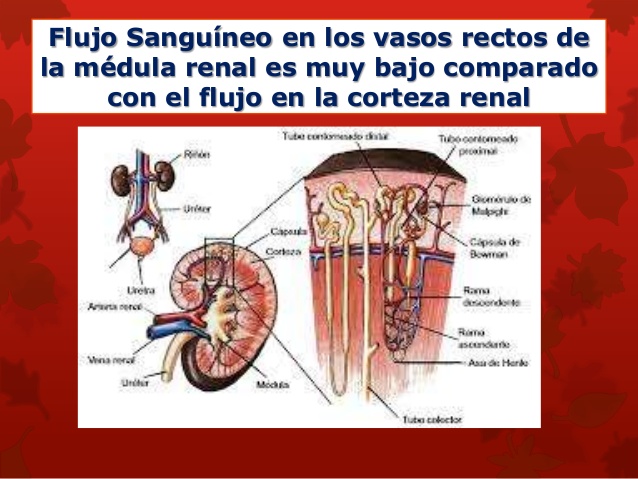
El flujo sanguíneo en los vasos rectos de la médula renal es
muy bajo comparado con el flujo en la corteza renal
La parte externa del riñón, la corteza renal, recibe la mayor parte del flujo sanguíneo renal. El flujo sanguíneo en la médula renal supone solo el 1-2% del flujo sanguíneo renal total.
El flujo en la médula renal procede de una porción especializada del sistema capilar peritubular llamada vasos rectos.
Control fisiológico de la filtración glomerular y del flujo sanguíneo renal
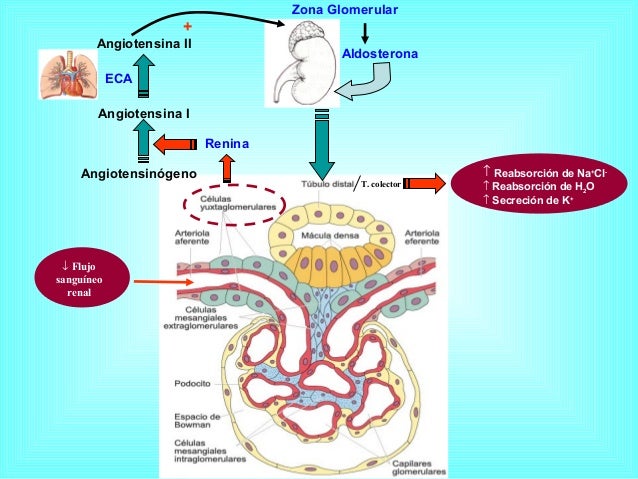
Los determinantes de la FG que son más variables y están sujetos al control fisiológico son la presión hidrostática glomerular y la presión coloidosmótica capilar glomerular. Estas variables, a su vez, están influenciadas por el sistema nervioso simpático, las hormonas y los autacoides (sustancias vasoactivas que liberan los riñones y actúan a nivel local) y otros controles de retroalimentación que son intrínsecos a los riñones
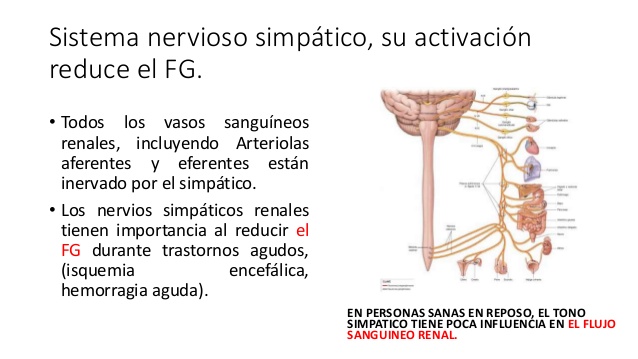
La intensa activación del sistema nervioso simpático reduce
la FG
Casi todos los vasos sanguíneos de los riñones, incluidas las arteriolas aferentes y eferentes, están muy inervados por fibras nerviosas simpáticas. La fuerte activación de los nervios simpáticos renales puede contraer las arteriolas renales y reducir el flujo sanguíneo renal y la FG.
La estimulación moderada o leve ejerce poca influencia sobre el flujo sanguíneo renal y la FG.
Los nervios simpáticos renales parecen más importantes para reducir la FG durante los trastornos agudos y graves que duran de varios minutos a unas pocas horas, como los provocados por las reacciones de defensa, la isquemia encefálica o la hemorragia grave.
Control hormonal y por autacoides de la circulación renal
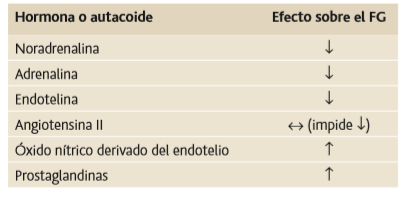
hormonas y autacoides pueden influir en la FG y en el flujo sanguíneo renal
Las hormonas que constriñen las arteriolas aferentes y eferentes, lo que reduce la FG y el flujo sanguíneo renal, son la noradrenalina y la adrenalina liberadas por la médula suprarrenal.
Las concentraciones sanguíneas de estas hormonas van generalmente paralelas a la actividad del sistema nervioso simpático; luego la noradrenalina y la adrenalina ejercen escasa influencia sobre la hemodinámica renal excepto en condiciones extremas, como una hemorragia grave.
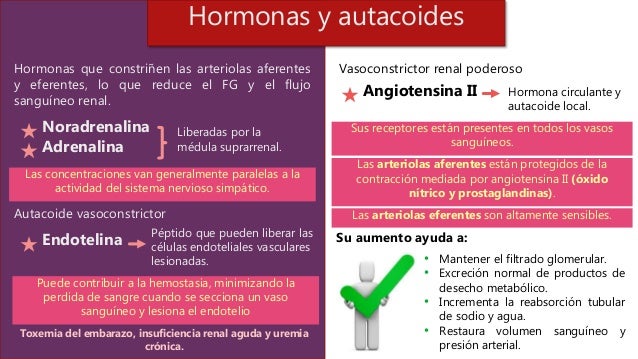
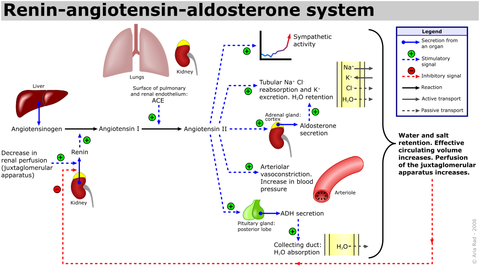
Un vasoconstrictor renal poderoso, la angiotensina II, puede considerarse una hormona circulante y un autacoide local porque se forma en los riñones y en la circulación sistémica.
Los receptores para angiotensina II están presentes prácticamente en todos los vasos sanguíneos.
No obstante, los vasos sanguíneos preglomerulares, en especial las arteriolas aferentes, parecen estar relativamente protegidos de la contracción mediada por angiotensina II en la mayoría de los estados fisiológicos asociados con la activación del sistema renina-angiotensina (p. ej., durante una dieta baja en sodio o una presión de perfusión renal reducida debida a estenosis de la arteria renal.
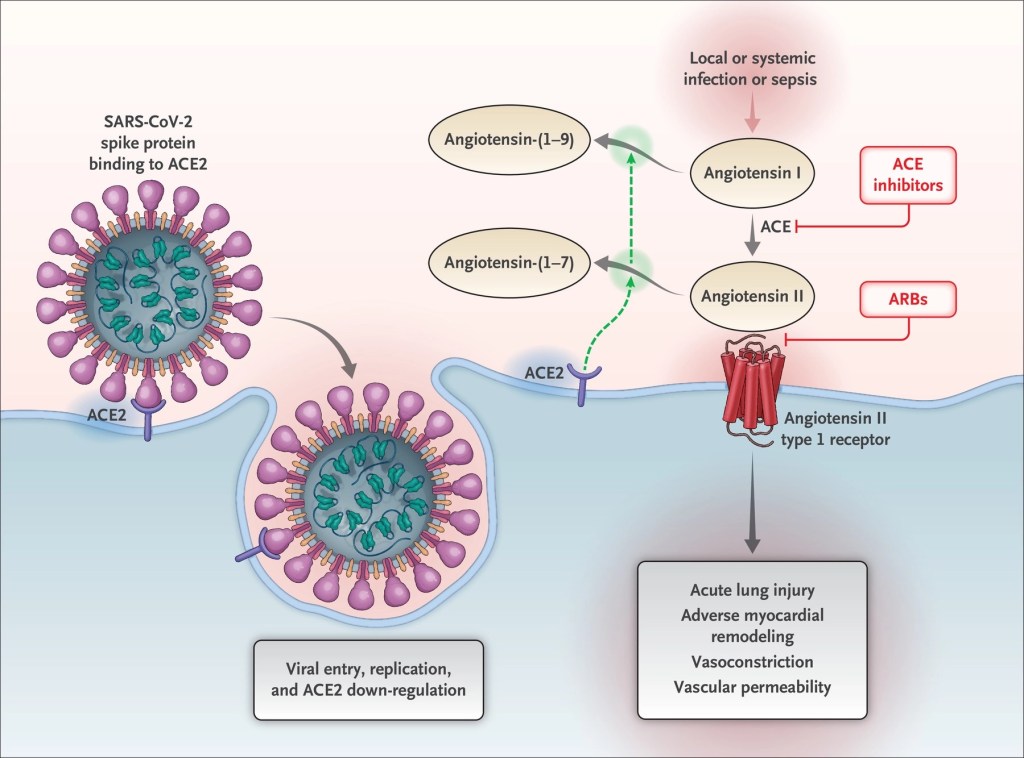
Debido a que la angiotensina II contrae sobre todo las arteriolas eferentes en la mayoría de los estados fisiológicos,
las concentraciones de angiotensina II aumentadas elevan la presión hidrostática glomerular mientras
reducen el flujo sanguíneo renal.
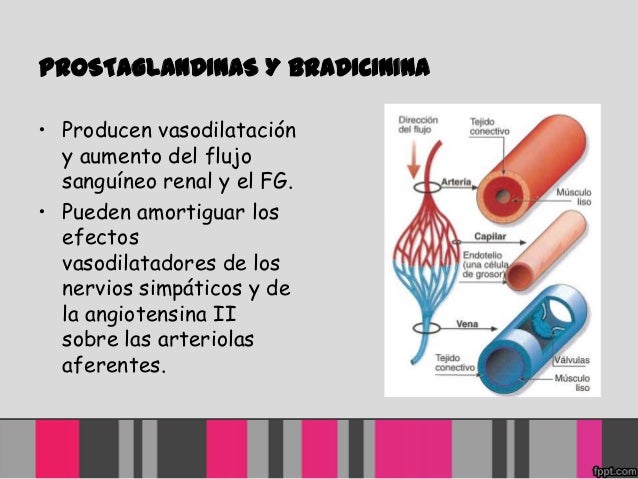
Las hormonas y los autacoides que producen vasodilatación y aumentan el flujo sanguíneo renal y la FG son las prostaglandinas (PGE2 y PGI2) y la bradicinina; amortiguan los efectos vasoconstrictores de los nervios simpáticos o de la angiotensina II, en especial sus efectos constrictores sobre las arteriolas aferentes.
Al oponerse a la vasoconstricción de las arteriolas aferentes, las prostaglandinas pueden ayudar a evitar reducciones excesivas de la FG y del flujo sanguíneo renal.
Autorregulación de la FG y del flujo sanguíneo renal
Los mecanismos de retroalimentación intrínsecos de los riñones mantienen normalmente el flujo sanguíneo renal y la FG relativamente constantes, a pesar de cambios acentuados en la presión arterial sistémica.
La principal función de la autorregulación del flujo sanguíneo en la mayoría de los tejidos diferentes a los riñones es mantener el reparto de oxígeno y nutrientes en valores normales y la extracción de los productos de desecho del metabolismo, a pesar de los cambios en la presión arterial.
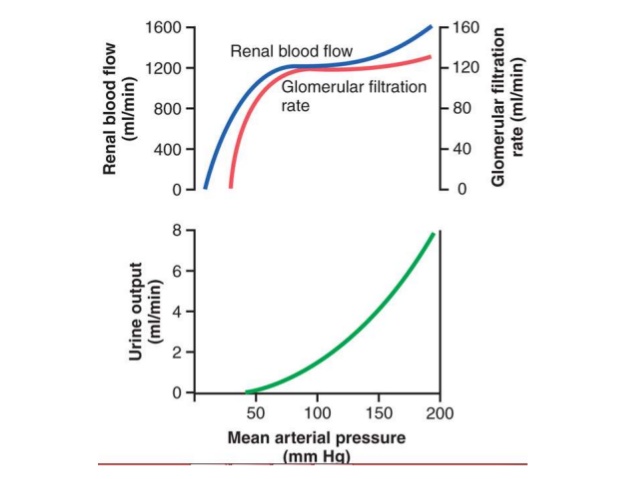
La FG permanece normalmente autorregulada (es decir, relativamente constante) a pesar de las fluctuaciones considerables de la presión arterial que se producen durante las actividades usuales de
una persona.
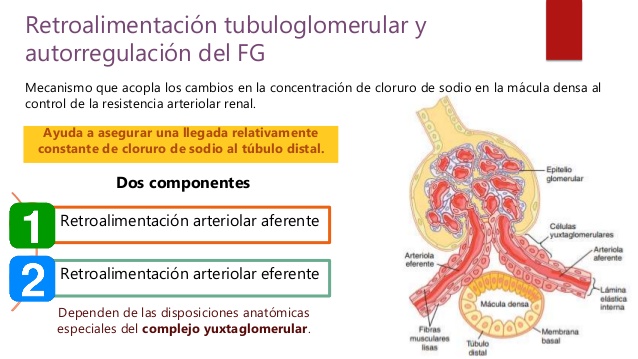
Retroalimentación tubuloglomerular y autorregulación de la
FG
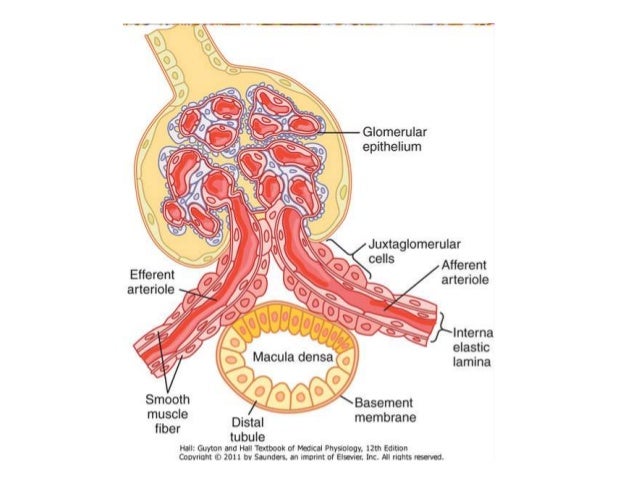
Los riñones tienen un mecanismo especial de retroalimentación que acopla los cambios en la concentración de cloruro de sodio en la mácula densa al control de la resistencia arteriolar renal y la
autorregulación de la FG.
Esta retroalimentación ayuda a asegurar una llegada relativamente constante de cloruro de sodio al túbulo distal y ayuda a evitar las fluctuaciones falsas en la excreción renal que de otro modo tendrían lugar.
En muchas circunstancias, esta retroalimentación autorregula el flujo sanguíneo renal y la FG en paralelo.

Autorregulación miógena del flujo sanguíneo renal y de la FG
El estiramiento de la pared vascular permite un mayor movimiento de los iones calcio desde el líquido extracelular hacia las células, lo que provoca su contracción por medio de los mecanismos.
Esta contracción impide una distensión excesiva de la pared y al mismo
tiempo, mediante un aumento de la resistencia vascular, ayuda a impedir un aumento excesivo del
flujo sanguíneo renal y de la FG cuando la presión arterial aumenta.
Aunque el mecanismo miógeno opera probablemente en la mayoría de las arteriolas del cuerpo, su importancia en la autorregulación del flujo sanguíneo renal y de la FG ha sido cuestionada por algunos fisiólogos porque este mecanismo sensible a la presión no tiene medio de detectar directamente por sí mismo cambios en el flujo sanguíneo renal ni en la FG.