Hormonas metabólicas tiroideas
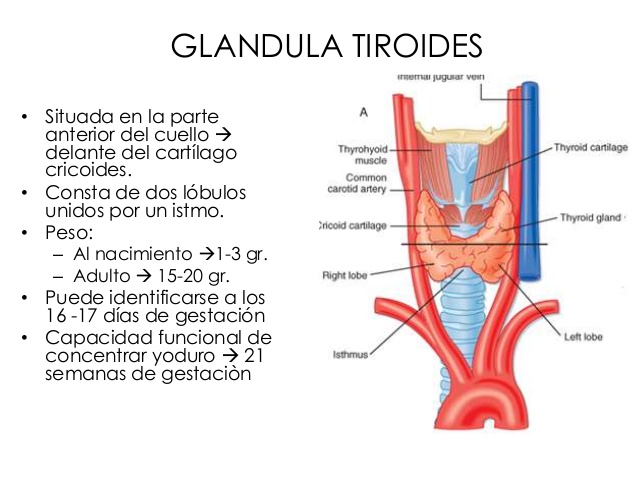
La glándula tiroides, situada justo por debajo de la laringe y a ambos lados y por delante de la tráquea, es una de las glándulas endocrinas más grandes, con un peso que oscila entre 15 y 20 g en los adultos sanos.
El tiroides secreta dos hormonas importantes, la tiroxina y la triyodotironina, conocidas a menudo como T4 y T3, respectivamente. Ambas inducen un notable aumento del
metabolismo del organismo. La ausencia completa de secreción tiroidea provoca con frecuencia
descensos metabólicos de hasta un 40-50% inferiores al valor normal, mientras que la secreción
excesiva incrementa el metabolismo en hasta el 60-100% por encima de lo normal.
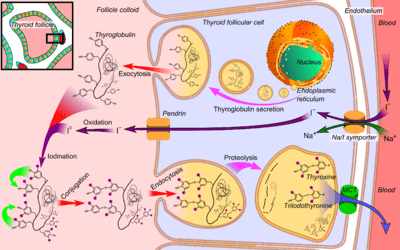
Síntesis y secreción de las hormonas metabólicas
tiroideas

Alrededor del 93% de las hormonas con actividad metabólica secretadas por la glándula tiroides
corresponde a tiroxina y el 7% restante, a triyodotironina.
Estas funciones son cualitativamente similares, aunque difieren en la rapidez y la
intensidad de la acción.
La triyodotironina es unas cuatro veces más potente que la tiroxina, si bien se detecta una cantidad mucho menor en la sangre y su duración es más breve.
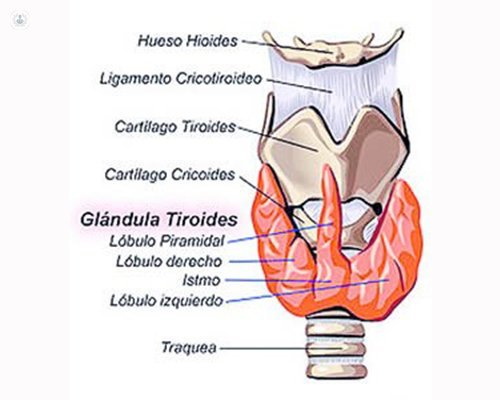
Anatomía fisiológica de la glándula tiroides
La glándula tiroides se compone de un elevado número de
folículos cerrados (100 a 300 μm de diámetro), que están repletos de una sustancia secretora denominada coloide y revestidos por células epiteliales cúbicas que secretan a la luz de los folículos.
El componente principal del coloide es una glucoproteína de gran tamaño, la tiroglobulina, cuya molécula contiene las hormonas tiroideas.
Cuando la secreción se encuentra en los folículos, la sangre debe absorberla de nuevo a través del epitelio folicular para que pueda actuar en el organismo.

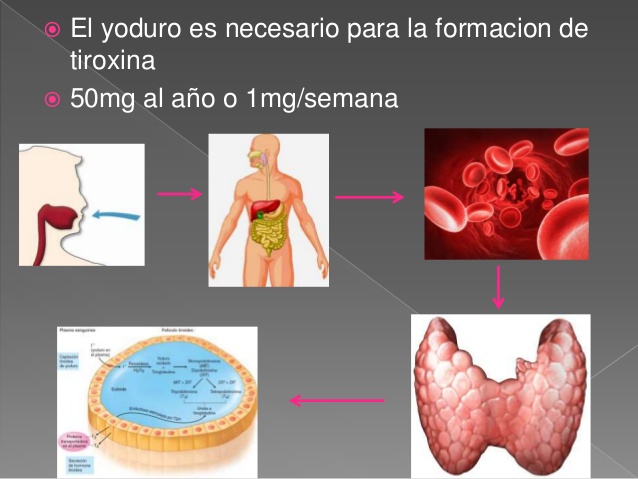
El yoduro es necesario para la formación de tiroxina
Para formar una cantidad normal de tiroxina se precisan al año unos 50 mg de yodo (ingerido en forma de yoduros) o el equivalente a 1 mg/semana. Para impedir la deficiencia de yodo, se añade una parte de yoduro sódico por cada 100.000 partes de cloruro sódico a la sal de mesa común.
Destino de los yoduros ingeridos
Los yoduros ingeridos por vía oral se absorben desde el tubo digestivo hasta la sangre de la misma
forma que los cloruros
Bomba de yoduro: el simportador del yoduro de sodio (atrapamiento de yoduro)
La primera etapa de la formación de las hormonas tiroideas consiste en el transporte de los yoduros desde la sangre hasta las células y los folículos de la glándula tiroides.
La membrana basal de estas células posee la capacidad específica de bombear de forma activa el yoduro al interior celular.
Este bombeo se consigue mediante la acción de un simportador del yoduro
de sodio, que cotransporta el ion yoduro a lo largo de dos iones sodio a través de la membrana basolateral (plasma) a la célula.
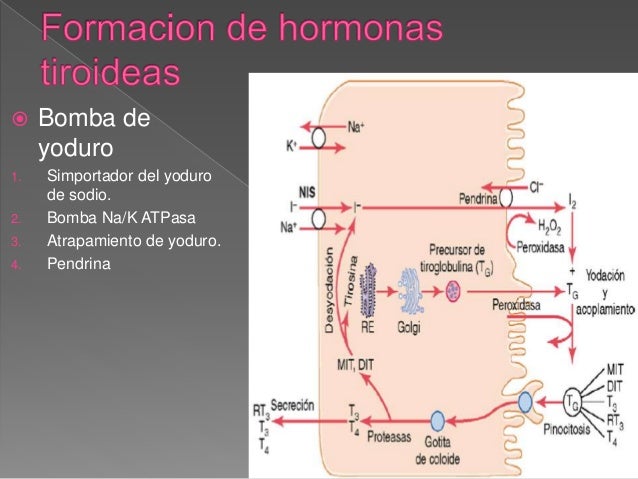
El proceso de concentración de yoduro en la célula se denomina atrapamiento de yoduro. En una glándula normal, la bomba de yoduro concentra esta sustancia hasta que su concentración supera en 30 veces la de la sangre.
El yoduro es transportado fuera de las células tiroideas a través de la membrana apical hacia el folículo por una molécula de contratransporte de cloruro-yoduro denominada pendrina.
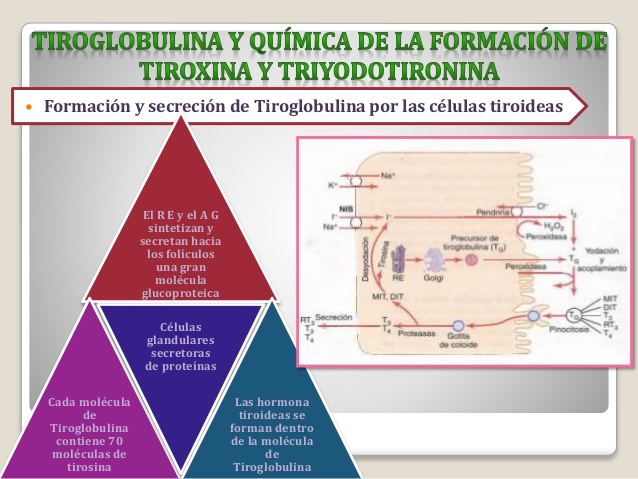
Tiroglobulina y química de la formación de tiroxina y
triyodotironina
Formación y secreción de tiroglobulina por las células tiroideas
Las células tiroideas constituyen un ejemplo típico de células glandulares secretoras de proteínas.
El retículo endoplásmico y el aparato de Golgi sintetizan y secretan hacia los folículos una gran molécula glucoproteica denominada tiroglobulina, con un peso molecular aproximado de 335.000.
Cada molécula de tiroglobulina contiene unas 70 moléculas del aminoácido tirosina, que es el sustrato principal que se combina con el yodo para dar lugar a las hormonas tiroideas.
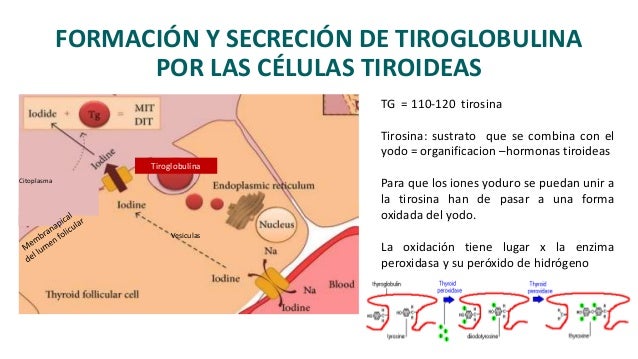
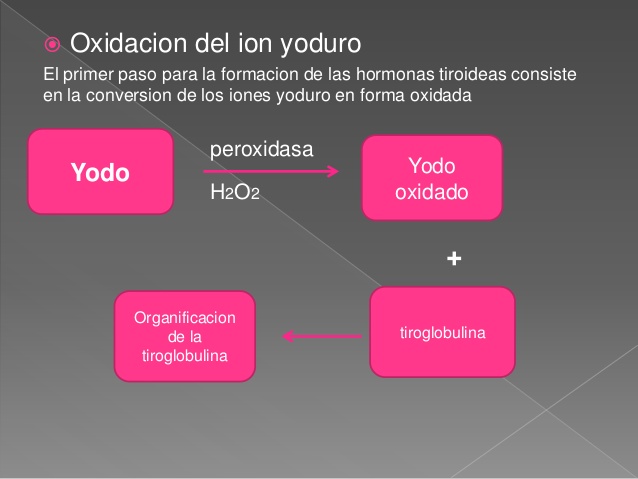
Oxidación del ion yoduro
El primer paso crítico para la formación de las hormonas tiroideas consiste en la conversión de los iones yoduro en una forma oxidada del yodo, bien en yodo naciente (I0), bien en I3 –, que luego puede combinarse directamente con el aminoácido tirosina. La oxidación del yodo depende de la enzima
peroxidasa y su peróxido de hidrógeno acompañante, que constituyen un potente sistema capaz de oxidar los yoduros.
Yodación de la tirosina y formación de las hormonas tiroideas: «organificación» de la tiroglobulina
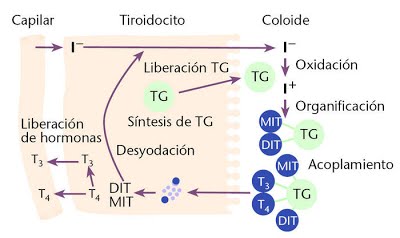
La unión del yodo a la molécula de tiroglobulina recibe el nombre de organificación de la tiroglobulina. El yodo oxidado (incluso en forma molecular) se une directamente, aunque con lentitud, al aminoácido tirosina. No obstante, en las células tiroideas el yodo oxidado se asocia a la enzima tiroidea peroxidasa
A medida que la tiroglobulina se libera del aparato de Golgi o se secreta al folículo
a través de la membrana apical de la célula, el yodo se fija a alrededor de la sexta parte de las tirosinas contenidas en la molécula de tiroglobulina.
El principal producto hormonal de la reacción de acoplamiento es la molécula tiroxina (T4), que se forma cuando se unen dos moléculas de diyodotirosina; la tirosina forma parte aún de la molécula de tiroglobulina.
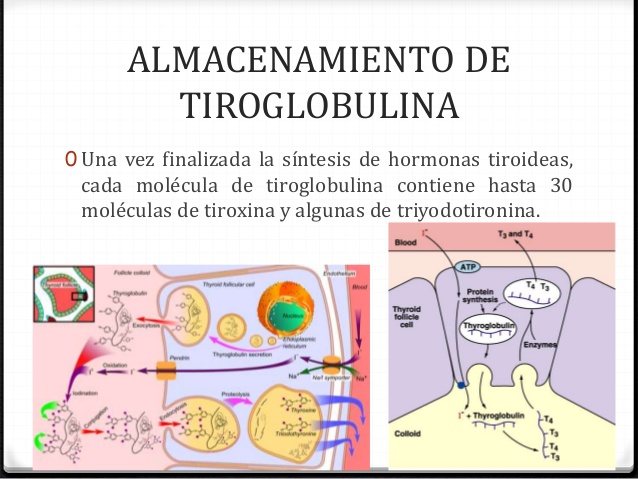
Almacenamiento de la tiroglobulina
La glándula tiroides es la única glándula endocrina que posee la capacidad de almacenar grandes cantidades de hormona. Una vez finalizada la síntesis de las hormonas tiroideas, cada molécula de tiroglobulina contiene hasta 30 moléculas de tiroxina y algunas de triyodotironina.
De esta forma, los folículos pueden almacenar una cantidad de hormona tiroidea suficiente para cubrir las necesidades normales del organismo durante 2 o 3 meses.
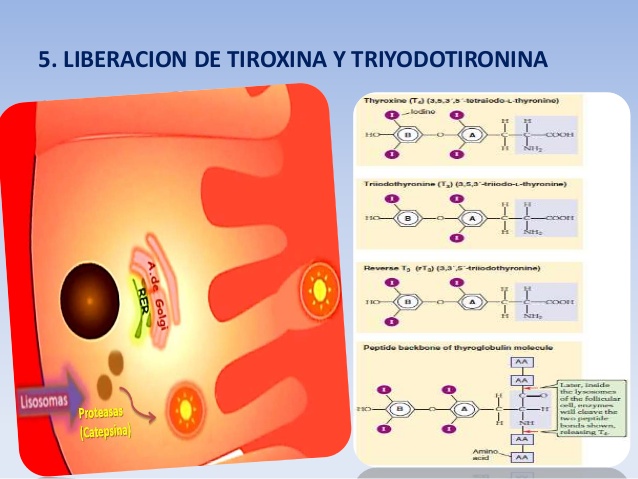
Liberación de tiroxina y triyodotironina del tiroides
La mayor parte de la tiroglobulina no se libera a la sangre circulante, sino que es preciso que la tiroxina y triyodotironina se escindan de la molécula de tiroglobulina; a continuación, ambas se secretan en forma libre. Este proceso tiene lugar por el siguiente mecanismo: la superficie apical de las células tiroideas emite extensiones en forma de seudópodos que rodean a pequeñas porciones del coloide, constituyendo vesículas de pinocitosis, que alcanzan la punta de la célula tiroidea.
A continuación, los lisosomas del citoplasma celular se funden de inmediato con estas vesículas y forman otras vesículas digestivas que contienen enzimas procedentes de los lisosomas mezcladas con el coloide.
Varias enzimas proteinasas digieren las moléculas de tiroglobulina, y liberan la tiroxina y la triyodotironina, que se difunden entonces a través de la base de la célula tiroidea, hacia los capilares circundantes, y de este modo pasan a la sangre.
Secreción diaria de tiroxina y de triyodotironina
En condiciones normales, alrededor del 93% de la hormona tiroidea liberada por la glándula tiroides corresponde a tiroxina y solo el 7% es triyodotironina. No obstante, en los días siguientes, la mitad de la tiroxina se desyoda con lentitud y forma más triyodotironina.
Transporte de tiroxina y triyodotironina a los tejidos
La tiroxina y la triyodotironina están unidas a proteínas plasmáticas

Cuando acceden a la sangre, más del 99% de la tiroxina y la triyodotironina se combina de inmediato con diversas proteínas plasmáticas, todas ellas sintetizadas por el hígado.
Estas proteínas son, ante
todo, la globulina fijadora de la tiroxina y, en menor medida, la prealbúmina y la albúmina fijadora
de la tiroxina.
La tiroxina y la triyodotironina se liberan lentamente a las células de los tejidos
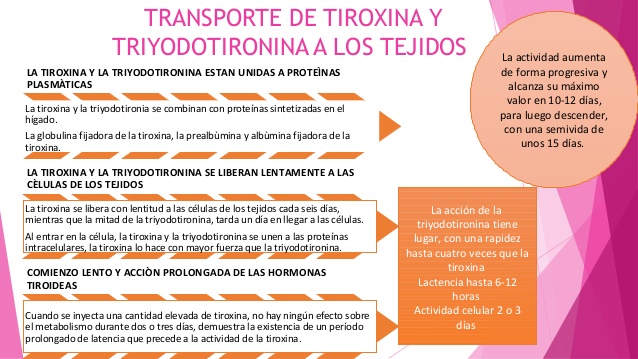
Debido a la gran afinidad de las proteínas de unión plasmáticas por las hormonas tiroideas, estas
sustancias, en concreto la tiroxina, se liberan con lentitud a las células de los tejidos.
La mitad de la tiroxina presente en la sangre se libera a las células de los tejidos cada 6 días aproximadamente, mientras que la mitad de la triyodotironina, dada su menor afinidad, tarda 1 día en llegar a las células
Comienzo lento y acción prolongada de las hormonas tiroideas
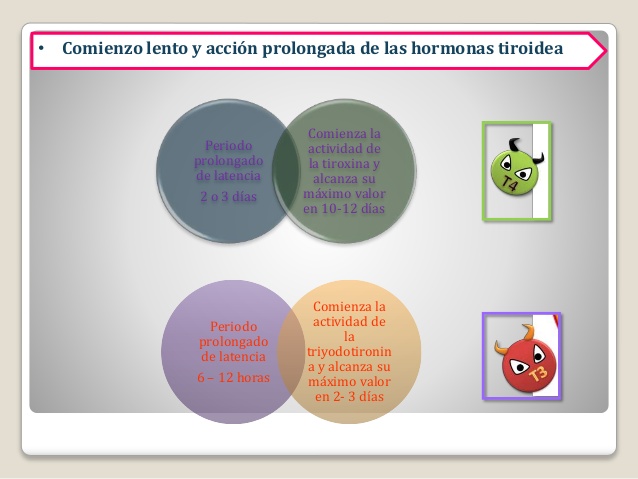
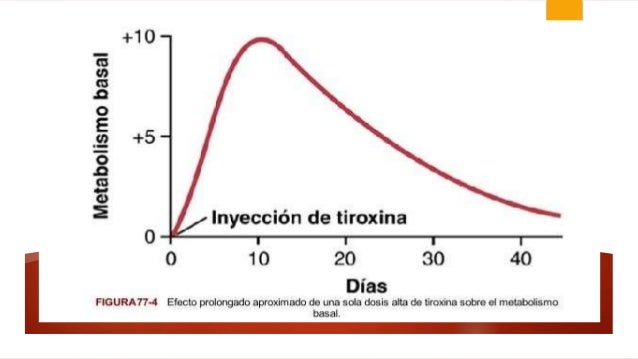
Cuando se inyecta una cantidad elevada de tiroxina a una persona, no se percibe ningún efecto sobre
el metabolismo durante 2 o 3 días, lo que demuestra la existencia de un período prolongado de
latencia que precede a la actividad de la tiroxina. Cuando esta actividad comienza, luego aumenta de
forma progresiva y alcanza su máximo valor en 10-12 días
Las acciones de la triyodotironina tienen lugar con una rapidez hasta cuatro veces mayor que las de la tiroxina; el período de latencia se acorta hasta 6-12 h y la actividad celular máxima se alcanza en 2 o 3 días.
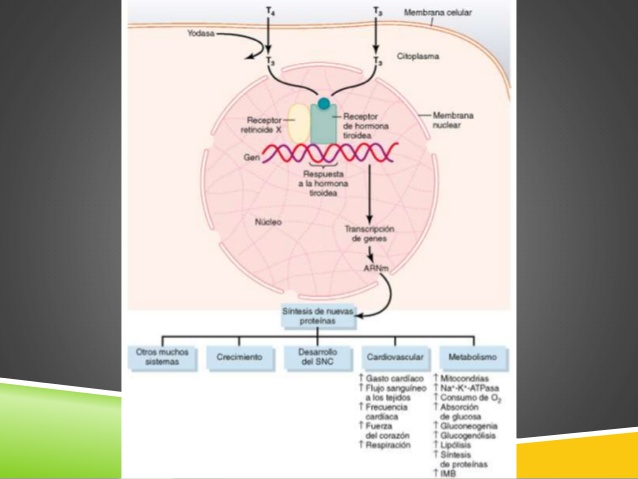
Funciones fisiológicas de las hormonas tiroideas
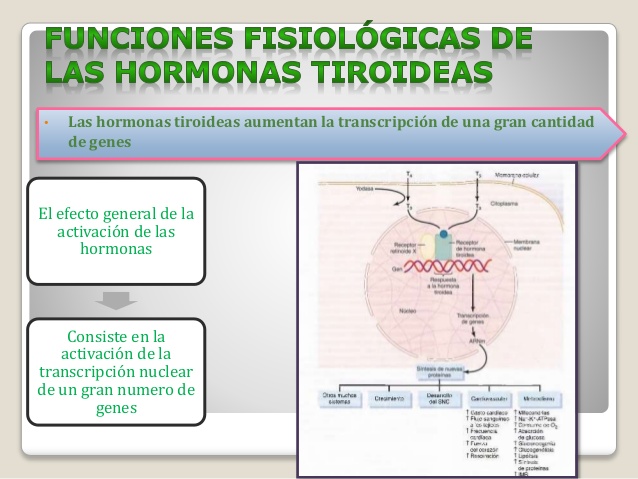
Las hormonas tiroideas aumentan la transcripción de una gran cantidad de genes
El efecto general de las hormonas tiroideas consiste en la activación de la transcripción nuclear de un gran número de genes.
Por consiguiente, en casi todas las células del organismo se sintetiza una elevada proporción de enzimas proteicas, proteínas estructurales, proteínas transportadoras y otras sustancias.
Casi toda la tiroxina secretada por el tiroides se convierte en triyodotironina
Antes de actuar sobre los genes e incrementar la transcripción genética, gran parte de la tiroxina liberada pierde un yoduro y se forma triyodotironina. Los receptores intracelulares de hormona tiroidea poseen una gran afinidad por la triyodotironina
Las hormonas tiroideas activan receptores nucleares
Los receptores de hormona tiroidea se encuentran unidos a las cadenas genéticas de ADN o junto a ellas.
El receptor suele formar un heterodímero con el receptor retinoide X (RXR) en los elementos específicos de respuesta a la hormona tiroidea del ADN. Después de unirse a esta hormona, los receptores se activan e inician el proceso de transcripción. A continuación, se forma una cantidad elevada de ARN mensajero de distintos tipos, seguido en unos minutos u horas de la traducción del ARN en los ribosomas citoplásmicos, para formar cientos de proteínas intracelulares nuevas.
Las hormonas tiroideas parecen tener también efectos celulares no genómicos que son independientes de sus efectos en la transcripción génica. Por ejemplo, algunos efectos de las hormonas tiroideas tienen lugar en cuestión de minutos, con demasiada rapidez para poder explicarse por los cambios en la síntesis proteica, y no se ven afectados por inhibidores de transcripción y traducción génica.

Las hormonas tiroideas aumentan la actividad metabólica celular
Las hormonas tiroideas incrementan las actividades metabólicas de casi todos los tejidos del organismo.
El metabolismo basal se incrementa entre el 60 y el 100% por encima de su valor normal cuando las concentraciones hormonales son altas. La velocidad de utilización de los alimentos como fuente de energía se encuentra muy acelerada. Aunque la síntesis de proteínas aumenta, también lo hace el catabolismo proteico. La velocidad de crecimiento de las personas jóvenes experimenta una
gran aceleración.
Los procesos mentales se estimulan y las actividades de las demás glándulas
endocrinas se potencian.
Las hormonas tiroideas incrementan el número y la actividad de las mitocondrias
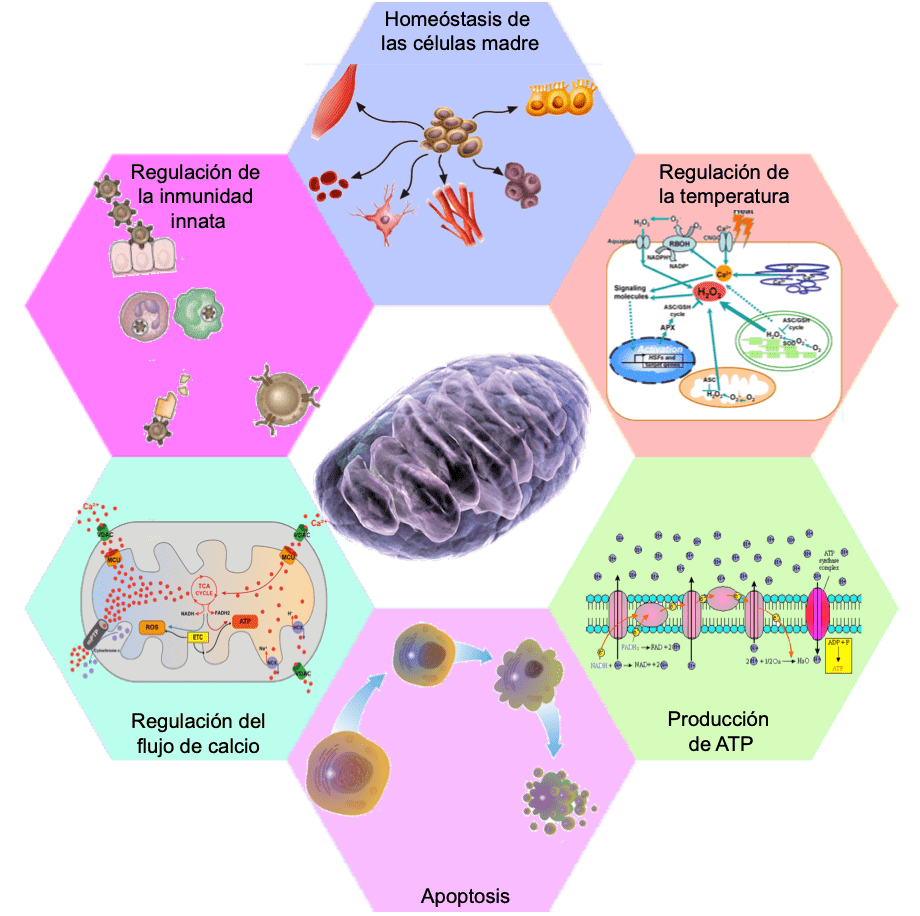
Una de las enzimas que aumentan en respuesta a la hormona tiroidea es la Na+-K+-ATPasa; a su vez,
este aumento de la actividad potencia el transporte de los iones sodio y potasio a través de la
membrana celular de determinados tejidos.
Este proceso requiere energía e incrementa la cantidad de
calor producida por el organismo, por lo que se ha propuesto que quizá constituya uno de los
mecanismos mediante los cuales la hormona tiroidea eleva el metabolismo

Efecto de las hormonas tiroideas sobre el crecimiento
La hormona tiroidea ejerce efectos generales y específicos sobre el crecimiento. Por ejemplo, se sabe desde hace bastante tiempo que la hormona tiroidea es esencial para la metamorfosis del renacuajo en rana.
En la especie humana, el efecto de la hormona tiroidea sobre el crecimiento se manifiesta sobre todo en los niños en edad de desarrollo.
Un efecto importante de la hormona tiroidea consiste en el estímulo del crecimiento y del
desarrollo del cerebro durante la vida fetal y en los primeros años de vida posnatal.
Si el feto no posee cantidades suficientes de hormona tiroidea, el crecimiento y la maduración del cerebro antes y después del nacimiento se retrasarán y su tamaño será más pequeño de lo normal.
Efectos de las hormonas tiroideas sobre funciones corporales
específicas
Estimulación del metabolismo de los hidratos de carbono
La hormona tiroidea estimula casi todas las fases del metabolismo de los hidratos de carbono, entre
ellos, la rápida captación de glucosa por las células, el aumento de la glucólisis, el incremento de la
gluconeogenia, una mayor absorción en el tubo digestivo e incluso una mayor secreción de insulina,
con sus efectos secundarios sobre el metabolismo de los hidratos de carbono.

Estimulación del metabolismo de los lípidos
La hormona tiroidea también potencia casi todos los aspectos del metabolismo de los lípidos. En
concreto, los lípidos se movilizan con rapidez del tejido adiposo, lo que disminuye los depósitos de
grasas del organismo en mayor medida que en casi todos los demás tejidos

Mayor necesidad de vitaminas
Dado que la hormona tiroidea incrementa la cantidad de numerosas enzimas corporales y que las
vitaminas suponen una parte esencial de algunas enzimas o coenzimas, la hormona tiroidea aumenta
las necesidades de vitaminas. Por
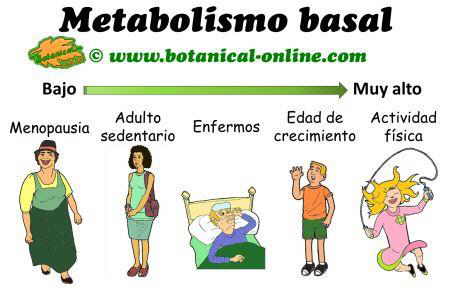
Aumento del metabolismo basal
La hormona tiroidea aumenta el metabolismo de casi todas las células del organismo, por lo que, en
cantidades excesivas, tiende a elevar el metabolismo basal hasta un 60 a un 100% por encima de las
cifras normales. Por el contrario, cuando no se produce hormona tiroidea, el metabolismo basal
disminuye hasta la mitad de lo normal.

Los grandes aumentos de la concentración de hormona tiroidea casi siempre producen
adelgazamiento, mientras que su disminución marcada se asocia en la mayoría de los casos a una
ganancia ponderal; sin embargo, no siempre se producen estos efectos, ya que la hormona tiroidea
también incrementa el apetito, lo que compensa el cambio metabólico
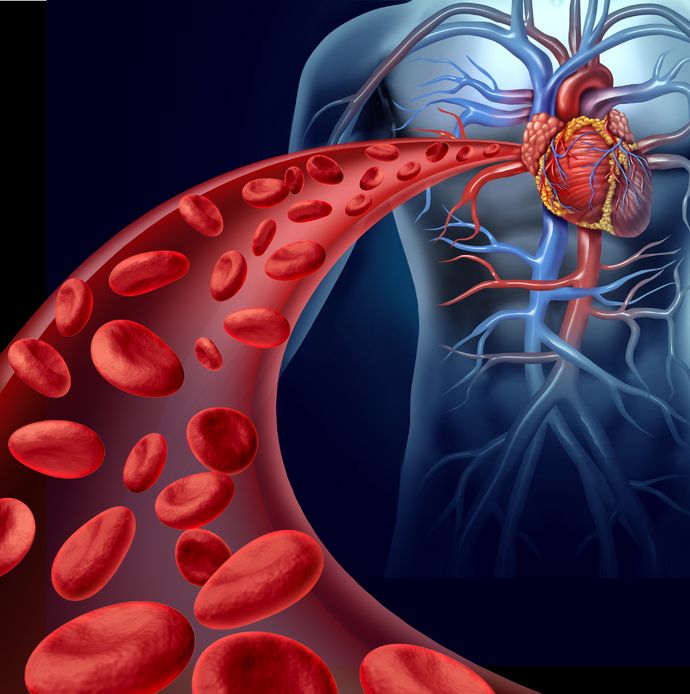
El aumento del metabolismo en los tejidos acelera la utilización de oxígeno e induce la liberación de
cantidades excesivas de productos metabólicos finales a partir de los tejidos. Estos efectos dilatan los
vasos de casi todos los tejidos orgánicos, elevando así el flujo sanguíneo. La elevación es más
acusada en la piel, debido a la mayor necesidad de eliminar el calor del organismo
Bajo la influencia de la hormona tiroidea, la frecuencia cardíaca se eleva mucho más de lo que cabría esperar por el incremento del gasto cardíaco.
Este efecto tiene especial importancia, ya que la frecuencia cardíaca es uno de los signos físicos en los que se basa el médico para determinar si un paciente produce una cantidad excesiva o
insuficiente de hormona tiroidea.
La mayor actividad enzimática inducida por la producción elevada de hormona tiroidea aumenta la fuerza del corazón cuando se secreta un ligero exceso de hormona tiroidea. Este efecto es análogo al incremento de la fuerza cardíaca que tiene lugar en presencia de febrícula y durante el ejercicio

La presión arterial media suele permanecer dentro de los valores normales tras la administración de
hormona tiroidea. No obstante, debido al aumento del flujo sanguíneo del tejido entre los latidos cardíacos, la presión diferencial tiende a elevarse; en el hipertiroidismo se observa un ascenso de la presión sistólica de 10-15 mmHg y una reducción similar de la presión diastólica.
El incremento del metabolismo eleva la utilización de oxígeno y la formación de dióxido de carbono; estos efectos activan todos los mecanismos que aumentan la frecuencia y la profundidad de
la respiración.

Además de aumentar el apetito y el consumo de alimentos, aspectos ya comentados, la hormona tiroidea favorece la secreción de los jugos digestivos y la motilidad del aparato digestivo.
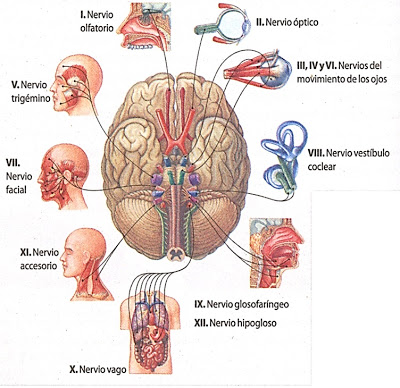
La hormona tiroidea acelera la función cerebral, aunque los procesos del pensamiento pueden estar disociados; por el contrario, la ausencia de hormona tiroidea disminuye la rapidez de la
función cerebral

Un ligero incremento de la hormona tiroidea desencadena una reacción muscular enérgica, pero cuando la cantidad de hormona resulta excesiva, los músculos se debilitan a causa del catabolismo excesivo de las proteínas.

Uno de los signos más característicos del hipertiroidismo consiste en un ligero temblor muscular.
Este síntoma no es comparable al temblor ostensible que se observa en la enfermedad de Parkinson o
en los escalofríos, ya que su frecuencia es rápida, de 10 a 15 veces por segundo. El temblor se percibe con facilidad colocando una hoja de papel sobre los dedos extendidos y observando el grado
de vibración del papel
La hormona tiroidea ejerce un efecto agotador sobre la musculatura y sobre el sistema nervioso central, por lo que las personas con hipertiroidismo suelen sentirse siempre cansadas, aunque les
resulte difícil conciliar el sueño debido a sus efectos excitantes sobre las sinapsis.
El aumento de la concentración de hormona tiroidea eleva la secreción de casi todas las demás glándulas endocrinas, aunque también la necesidad tisular de hormonas.
Por ejemplo, cuando se incrementa la secreción de tiroxina, lo hace también el metabolismo de la glucosa de casi todo el organismo, lo que se asocia a una mayor necesidad de secreción de insulina por el páncreas.

Efecto de las hormonas tiroideas sobre la función sexual
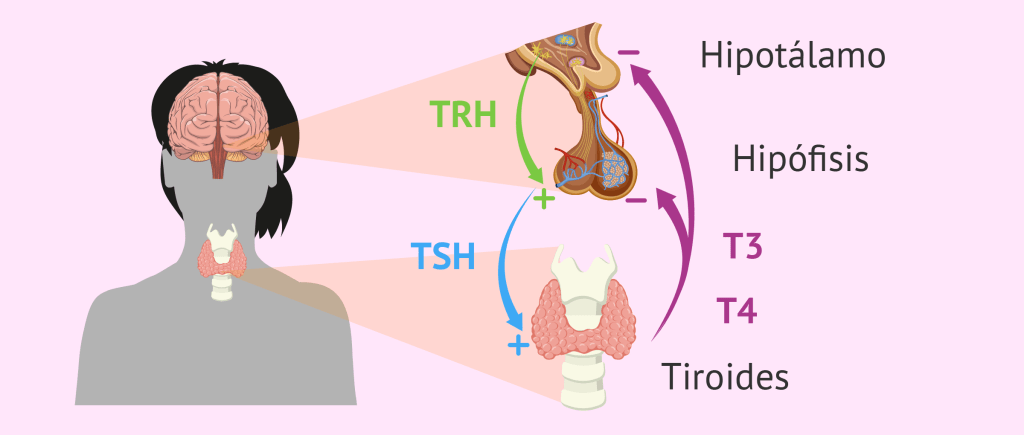
Regulación de la secreción de hormonas tiroideas
Con el fin de mantener una actividad metabólica normal en el organismo, es preciso que en todo
momento se secrete una cantidad adecuada de hormona tiroidea; para lograr este nivel ideal de
secreción existen mecanismos específicos de retroalimentación que operan a través del hipotálamo y de la adenohipófisis y que controlan la secreción tiroidea.
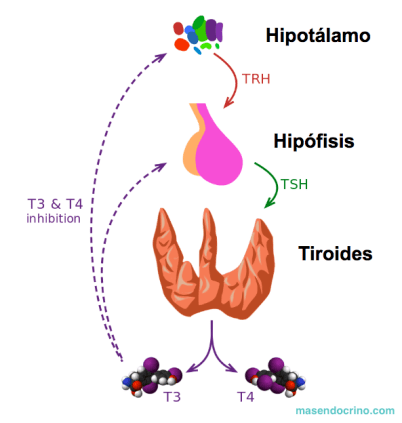
La TSH adenohipofisaria incrementa la secreción tiroidea
La TSH, denominada también tirotropina, es una hormona adenohipofisaria, una glucoproteína con un peso molecular de aproximadamente 28.000
incrementa la secreción de tiroxina y de triyodotironina por la glándula tiroides. Los efectos queejerce sobre esta glándula son los siguientes:
- Eleva la proteólisis de la tiroglobulina que se encuentra almacenada en los folículos, con lo que se
liberan hormonas tiroideas a la sangre circulante y disminuye la sustancia folicular. - Incrementa la actividad de la bomba de yoduro, que favorece el «atrapamiento del yoduro» por las
células glandulares, elevando en ocasiones la relación entre las concentraciones intra- y extracelular
de yodo en la sustancia glandular hasta ocho veces por encima de los valores normales. - Intensifica la yodación de la tirosina para formar hormonas tiroideas.
- Aumenta el tamaño y la actividad secretora de las células tiroideas.
- Incrementa el número de células tiroideas y transforma las células cúbicas en cilíndricas e induce el plegamiento del epitelio tiroideo en el interior de los folículos.
En resumen, la TSH estimula todas las actividades secretoras conocidas de las células glandulares
tiroideas.
El monofosfato de adenosina cíclico actúa como mediador del efecto estimulador de la TSH
La mayoría de los numerosos y variados efectos de la TSH sobre las células tiroideas obedecen a la activación del sistema de «segundo mensajero» del AMPc de la célula.
El primer acontecimiento de esta activación consiste en la unión de la TSH con sus receptores específicos de la membrana basal de la célula tiroidea. Se activa así la adenilato ciclasa de la membrana, lo que incrementa la formación de AMPc en la célula.
Por último, el AMPc actúa como segundo mensajero y activa la proteína cinasa, que produce múltiples fosforilaciones en toda la célula. El resultado es un aumento inmediato de la secreción de hormonas tiroideas y un crecimiento
prolongado del propio tejido de la glándula.
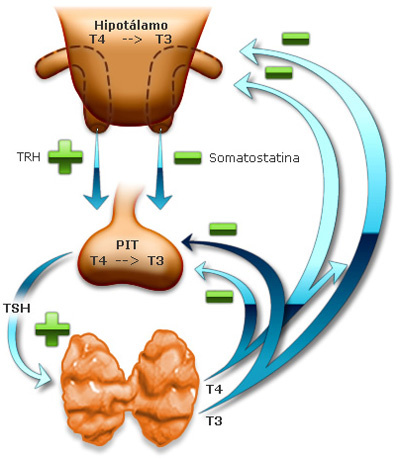
La secreción adenohipofisaria de TSH se encuentra regulada
por la tiroliberina procedente del hipotálamo
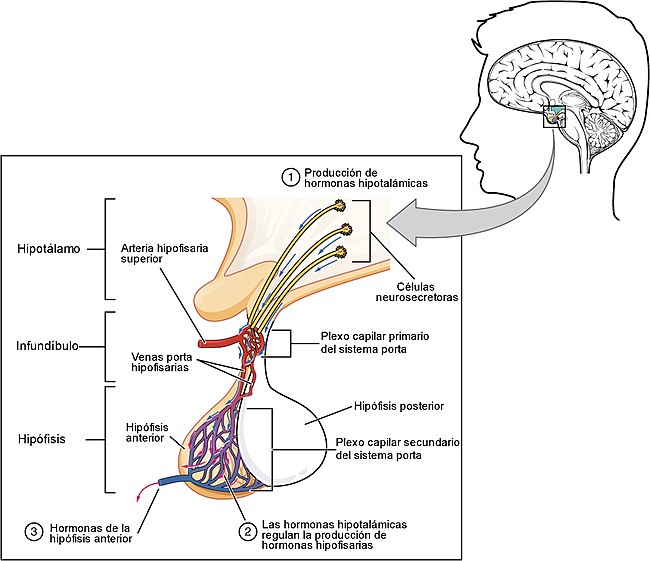
La secreción de TSH por la adenohipófisis está controlada por una hormona hipotalámica, la tiroliberina u hormona liberadora de tirotropina (TRH), secretada por las terminaciones nerviosas de la eminencia media del hipotálamo.
A continuación, los vasos porta hipotalámico-hipofisarios transportan la TRH desde la eminencia media hasta la adenohipófisis.
El mecanismo molecular mediante el cual la TRH estimula a las células adenohipofisarias secretoras de TSH para que sinteticen esta hormona consiste, en primer lugar, en su unión a los receptores de TRH de la membrana celular de la hipófisis.
Efectos del frío y de otros estímulos nerviosos sobre la secreción de TRH y TSH

Uno de los estímulos más conocidos de la secreción de TRH por el hipotálamo y, por consiguiente, de la secreción de TSH por la adenohipófisis es la exposición de un animal al frío.
Este efecto obedece casi con toda seguridad a la excitación de los centros hipotalámicos encargados de controlar la temperatura corporal.
Algunas reacciones emocionales también afectan a la producción de TRH y TSH, por lo querepercuten de forma indirecta en la secreción de las hormonas tiroideas.
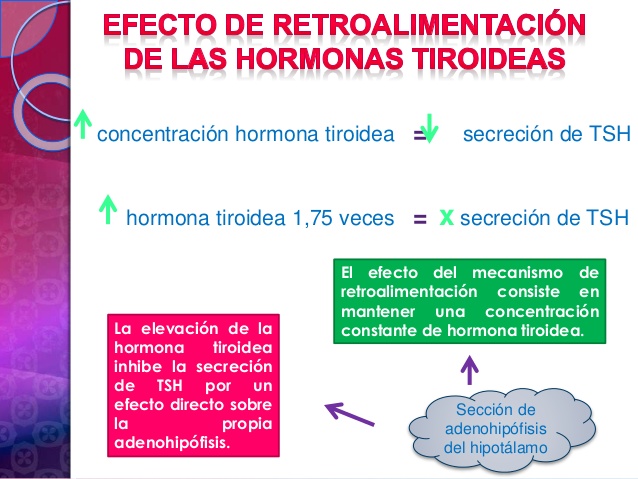
Efecto de retroalimentación de las hormonas tiroideas para
disminuir la secreción adenohipofisaria de TSH
El ascenso de la concentración de hormona tiroidea en los líquidos corporales reduce la secreción de TSH por la adenohipófisis, Cuando la secreción de hormona tiroidea aumenta hasta 1,75 veces los valores normales, la secreción de TSH cae hasta casi desaparecer. Este efecto depresor mediante retroalimentación apenas disminuye cuando se separa la adenohipófisis del hipotálamo

Las sustancias antitiroideas suprimen la secreción tiroidea
Los fármacos antitiroideos mejor conocidos son el tiocianato, el propiltiouracilo y las concentraciones elevadas de yoduros inorgánicos.
La misma bomba activa que transporta los iones yoduro al interior de las células tiroideas bombea además iones tiocianato, iones perclorato e iones nitrato. Por consiguiente, la administración de una concentración lo bastante elevada de tiocianato (o de alguno de los otros iones) inhibe de forma competitiva el transporte de yoduro a la célula y, por tanto, inhibe el mecanismo de atrapamiento del
yoduro.
El propiltiouracilo (junto con otros compuestos similares, como el metimazol y el carbimazol)
impide la formación de hormona tiroidea a partir del yoduro y la tirosina. El mecanismo de esta acción consiste, por una parte, en bloquear la enzima peroxidasa necesaria para la yodación de la tirosina y, por otra, en impedir el acoplamiento de dos tirosinas yodadas para formar tiroxina o
triyodotironina
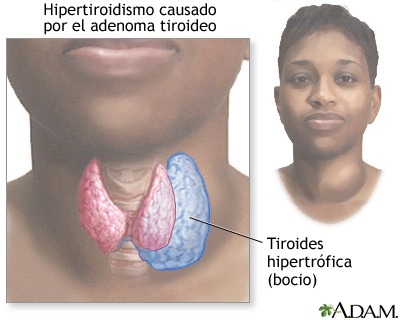
Enfermedades del tiroides

En la mayoría de los pacientes con hipertiroidismo se observa un aumento de tamaño de la glándula
tiroides, que llega a duplicarse o triplicarse, con una hiperplasia considerable y un plegamiento del
revestimiento de las células foliculares en los folículos, por lo que el número de células también aumenta de forma notable.
Los síntomas de hipertiroidismo deben resultar evidentes a partir de la exposición anterior de la
fisiología de las hormonas tiroideas:
- Estado de gran excitabilidad
- Intolerancia al calor
- Aumento de la sudoración
- Adelgazamiento leve o extremo (en ocasiones, hasta 45 kg)
- Grado variable de diarrea
- Debilidad muscular
- Nerviosismo u otros trastornos psíquicos
- Fatiga
- Extrema e incapacidad para conciliar el sueño
- temblor de las manos.

A menudo se inicia por autoinmunidad contra la glándula tiroides (enfermedad de Hashimoto), aunque en este caso la inmunidad no estimula a la glándula, sino que la destruye.
La glándula tiroides de casi todos estos pacientes sufre una «tiroiditis» autoinmunitaria, es decir, una inflamación del tiroides, que provoca su deterioro progresivo y, en última instancia, la fibrosis de la glándula, con una secreción escasa o nula de hormonas tiroideas
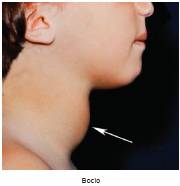
Bocio coloide endémico asociado a la deficiencia alimenticia de yodo
El término «bocio» se aplica a una glándula tiroides de gran tamaño

Bocio coloide idiopático no tóxico
Estas glándulas bociosas elaboran a veces cantidades normales
de hormona tiroidea, pero lo más común es que la secreción hormonal esté deprimida, como sucede
en el bocio coloide endémico.

El cretinismo se debe a un hipotiroidismo extremo sufrido durante la vida fetal, la lactancia o la infancia.
Esta enfermedad se caracteriza especialmente por la falta de crecimiento y por retraso mental. Puede deberse a la ausencia congénita de la glándula tiroides (cretinismo congénito), a que la glándula tiroides no sintetiza hormona tiroidea por un defecto genético de la glándula o una carencia de yodo en la alimentación (cretinismo endémico).
Algunos neonatos que carecen de glándula tiroides tienen un aspecto y una función normales, ya que recibieron cierta cantidad (aunque no suficiente) de hormona tiroidea de la madre durante la vida uterina; no obstante, varias semanas después de nacer, los movimientos del niño se hacen más lentos y el crecimiento físico y mental se retrasa considerablemente.